SARS-CoV-2 Zytokinfreisetzungssyndrom (Cytokine Release Syndrom (CRS))
Bei den meisten Patienten, die eine schwere COVID-19 entwickeln, klingen die Entzündungsprozesse nicht ab. Stattdessen entsteht ein Zytokinsturm, eine hyperinflammatorische Reaktion, die eine dysregulierte Aktivierung einer großen Anzahl von Immun- und Entzündungszellen beinhaltet.
Die IL-6-Spiegel steigen weiter an und auch die Spiegel von IL- 2, IL-7, IL-10, TNF-α, G-CSF, CXCL10, CCL2 und CCL3 sind bei COVID-19-Patienten deutlich erhöht. Die Anzahl der CD4+ und CD8+ T-Zellen ist bei COVID-19-Patienten antiproportional zu den Werten von TNF-alpha, IL-6 und IL-10. Die Expression der Erschöpfungsmarker PD-1 und HAVCR2 ist in diesen Zellen ebenfalls erhöht.Auf der anderen Seite ist bei schweren Fällen von COVID-19 die Anzahl der CD14+CD16+ entzündlichen Monozyten im peripheren Blut erhöht. CD14+CD16+ Monozyten wurden auch mit der Kawasaki-Krankheit in Verbindung gebracht, einer seltenen akuten entzündlichen Erkrankung der Arterien bei Kleinkindern, die kürzlich in Verbindung mit COVID-19 beobachtet wurde. Diese CD14+CD16+ Monozyten sind auch CD11b+ , CD14+ , CD16+ , CD68+ , CD80+ , CD163+ , CD206+ und sezernieren IL-6, IL-10 und TNF-alpha und tragen somit weiter zur Entzündung bei.
All diese Faktoren tragen zur Entwicklung eines Zytokinfreisetzungssyndroms oder Zytokinsturms bei, einer exzessiven Entzündungsreaktion, bei der Zytokine als Reaktion auf eine Infektion schnell in großen Mengen produziert werden. Der Zytokinsturm gilt als ein wichtiger Faktor, der zu ARDS und MODS beiträgt.
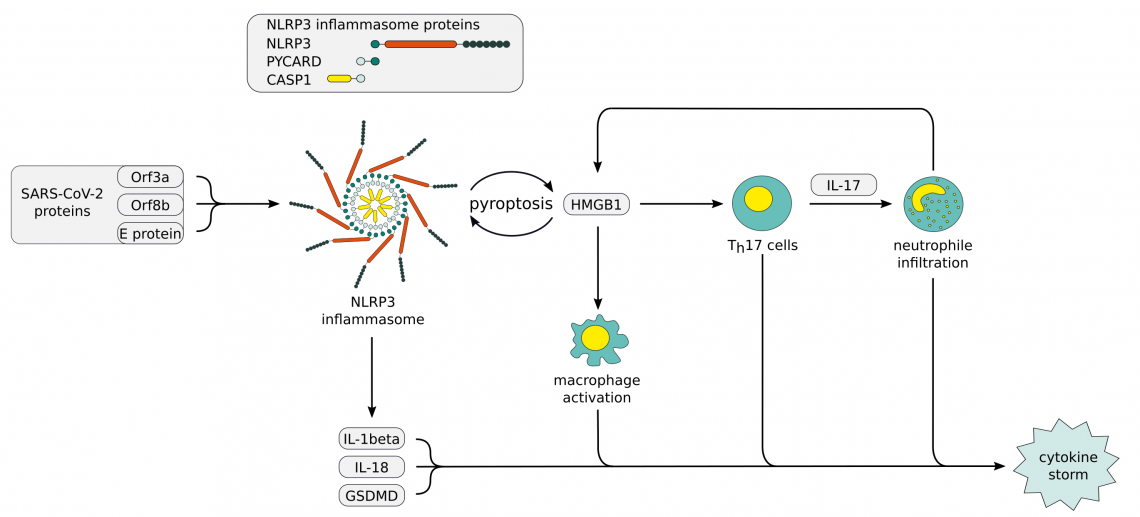
Es gibt Hinweise auf eine erhöhte Anfälligkeit für einen schweren Verlauf von COVID-19 aufgrund von lebensstilbedingten Low-Grade-Entzündungen oder genetischen Faktoren. Diese Faktoren können zu einer erhöhten Exposition gegenüber DAMPs (damage associated molecular patterns) und einer weiteren NLRP3-Inflammasom-Aktivierung führen. Einer der DAMPs, der der NLRP3-Inflammasom-Aktivierung nachgeschaltet ist, ist HMGB1. Es wird typischerweise in erhöhten Serumkonzentrationen während entzündlicher Ereignisse gefunden und wirkt als zentraler Mediator einer exzessiven Entzündungsreaktion bei viralen Infektionen. Es wird angenommen, dass HMGB1 über eine positive Rückkopplungsschleife, die die Induktion der IL-17-Produktion durch Th17-Zellen und die anschließende neutrophile Infiltration einschließt und zu einer weiteren NLRP3-Inflammasom-Aktivierung führt, einer der Hauptakteure des Zytokinsturms ist.
Das SARS-CoV-2 N-Protein löst die Aktivierung des Lektinwegs des Komplementsystems durch Interaktion mit der Mannose-bindenden Lektin (MBL)-assoziierten Serinprotease (MASP)2 aus. Freigesetzte lösliche N-Protein-Dimere interagieren mit MASP-2, was die Aktivierung von MASP-2 und die Aktivierung des Komplementsystems weiter beschleunigt. Die positive Rückkopplung durch Zelllyse und Freisetzung von N-Protein führt zu einem weiteren Anstieg von pro-inflammatorischen Zytokinen und einer Verschärfung des Zytokinsturms.
Neben der schädigenden Wirkung auf die Alveolarstruktur induzieren die inflammatorischen Zytokine IL-1 und TNF eine erhöhte Expression von HA-Synthase-2 (HAS2) in CD31+-Endothel, EpCAM+-Lungenalveolarepithelzellen und Fibroblasten. HAS2 katalysiert die Polymerisation von Hyaluronan, einer Komponente der extrazellulären Matrix, die Wasser bis zum 1000-fachen ihres Gewichts aufnehmen kann. Die Anhäufung dieses flüssigen Gelees in der geschädigten Lunge schränkt den Gasaustausch in der Lunge weiter ein und führt zu einer niedrigen Sauerstoffsättigung des Blutes.

Kostenlos: SARS-CoV-2 Handbuch
49 Seiten * Freier Download * Antibodies und Proteins * SARS-CoV-2 Lineages * Mutationen & Implikationen für NAbs
Mehr Infos und DownloadRelevante Antikörper:
- (2)
- (6)
- (2)
- (7)
- (1)
- (7)
- (2)
- (5)
- (8)
- (5)
- (8)
- (3)
- (2)
- (1)
- (2)
- (1)
- (2)
- (1)
- (2)
Relevante ELISA Kits:
(Pre-coated)
- (53)
- (6)
(Pre-coated)
- (25)
- (6)
(Pre-coated)
- (31)
- (5)
(Pre-coated)
- (16)
- (5)
(Pre-coated)
- (4)
- (5)
(Pre-coated)
- (8)
- (5)
(Pre-coated)
- (3)
- (5)
(Pre-coated)
- (4)
- (4)
Weitere COVID-19 DAMPs
Die Immunantwort auf eine SARS-CoV-2 Infektion wird neben HMGB1 auch durch weitere DAMPs bestimmt. Dies können endogene Proteine infizierter Zellen sein, die durch den Zelltod freigesetzt werden, modifizierte Komponenten der extrazellulären Matrix, oder DAMP-induzierte sekretierte Protein, die nachgelagert selbst als DAMPs wirken. Neben HMGB1 sind CIRBP, S100A8/A9 und SP-1 für COVID-19 charakteristische DAMPs.
SARS-CoV-2 DAMPs antibodies:
- (4)
- (12)
- (1)
- (3)
- (2)
SARS-CoV-2 DAMPs ELISA Kits:
(Pre-coated)
- (53)
- (6)
(Pre-coated)
- (6)
- (6)
(Pre-coated)
- (4)
- (5)
(Pre-coated)
- (10)
- (1)
(Pre-coated)
- (1)
Weitere Informationen und Produkte
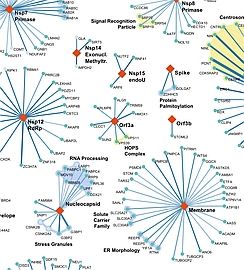
SARS-CoV Protein Interactome / poster and products
NLRP3 inflammasome, poster and products
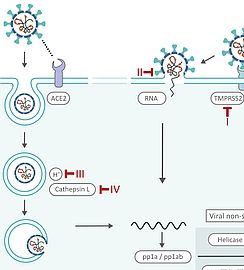
SARS-CoV-2 Life Cycle: Stages and Inhibition Targets
Coronavirus Expression Vectors and Cloning Vectors at genomics-online.com.
Referenzen
: "Imbalanced Host Response to SARS-CoV-2 Drives Development of COVID-19." in: Cell, Vol. 181, Issue 5, pp. 1036-1045.e9, (2020) (PubMed).: "ORF8 contributes to cytokine storm during SARS-CoV-2 infection by activating IL-17 pathway." in: iScience, Vol. 24, Issue 4, pp. 102293, (2021) (PubMed).
: "The trinity of COVID-19: immunity, inflammation and intervention." in: Nature reviews. Immunology, Vol. 20, Issue 6, pp. 363-374, (2020) (PubMed).
: "Severe COVID-19: NLRP3 Inflammasome Dysregulated." in: Frontiers in immunology, Vol. 11, pp. 1580, (2020) (PubMed).
: "The CD14+ CD16+ blood monocytes: their role in infection and inflammation." in: Journal of leukocyte biology, Vol. 81, Issue 3, pp. 584-92, (2007) (PubMed).
- Gao, T. et al. Highly pathogenic coronavirus N protein aggravates lung injury by MASP-2- mediated complement over-activation. medRxiv (2020). doi:10.1101/2020.03.29.20041962
- Fan, X. et al. Changes of Damage Associated Molecular Patterns in COVID-19 Patients. Infectious Diseaeses & Immunity (2021). doi:10.1097/01.id9.0000733572.40970.6c
- Zhang, D. et al. COVID-19 infection induces readily detectable morphological and inflammation-related phenotypic changes in peripheral blood monocytes, the severity of which correlate with patient outcome. medRxiv (2020). doi:10.1101/2020.03.24.20042655